En distintos estudios y cursos relacionados con la bioquímica se difunde que el metabolismo anaeróbico de la glucosa crea ácido láctico, al que se le puede atribuir carias cualidades como poder generar calambres en los músculos que se han ejercitado muy rápida e intensamente. No obstante, cuando se suelen explicar las reacciones de la ruta metabólica de la glucólisis en ausencia de oxígeno, finaliza con la conversión de piruvato en lactato, por la reacción donde la lactato deshidrogenasa interviene sin afectar, es decir, que el piruvato no se convierte en ácido láctico.
Por otro lado, en relación con el catabolismo anaeróbico de la glucosa, se tiene certeza de que va a provocar acidez, por esta razón es que la potente activación de este procedimiento metabólico tiene la capacidad de formar la conocida acidosis láctica, que no básicamente la obtención de un exceso de hidrogeniones presente con la creación de un exceso de lactato en condiciones de hipoxia tisular relacionada con los cambios de la función ventilatoria o cardiaca.
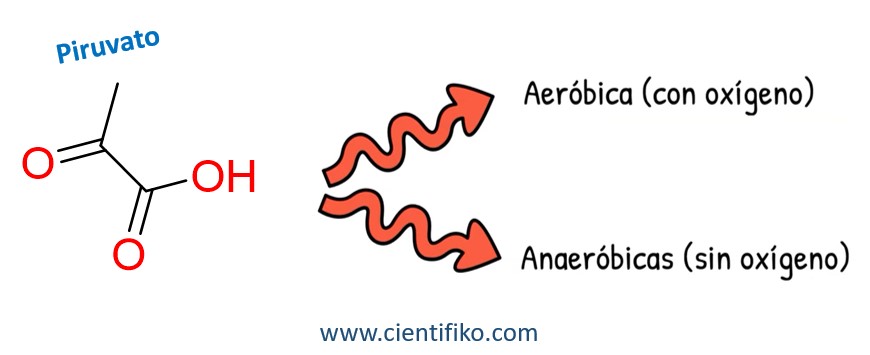
Table of Contents
¿Qué es la glucólisis?
Al igual que sucede frecuentemente en algunas patologías hepáticas, debido a que el hígado es el órgano fundamental que se ocupa de eliminar el lactato de la sangre para que sea transformado en glucosa. Además, los diferentes tóxicos como por ejemplo el etanol, el etilenglicol y otros más pueden afectan el metabolismo en relación con la producción excesiva de ácido láctico.
La glucólisis es un conjunto de reacciones consecutivas que obtienen energía de la glucosa al separarla en dos moléculas que se forman por tres carbonos que se conocen con el nombre de piruvato. La glucólisis se puede considerar entonces una vía metabólica cuya evolución ocurrió hace ya bastante tiempo y en la actualidad este proceso está muy presente en la gran mayoría de los organismos vivos del planeta.
La glucólisis es la primera etapa de este proceso de respiración celular en todos aquellos organismos que lo hacen para obtener energía que puedan aprovechar sus células. No obstante, el proceso de glucólisis no requiere necesariamente de oxígeno, por lo que la mayoría de los organismos que no utilizan oxígeno o anaerobios también se valen de esta vía. (1)
Fases de la glucólisis
Fase I
Los hidratos de carbono entran al organismo mediante la ingesta de alimentos como polisacáridos, de los cuales los más nombrados son lactosa, sacarosa, almidones y amilosa, glucógeno, alcohol, ácido láctico, y ácido pirúvico. La digestión de todas estas sustancias comienza en la boca por medio de la enzima conocida como ptialina o alfa-amilasa, luego sigue con la amilasa pancreática.
De esta manera es que la totalidad de los hidratos de carbono terminarán en el intestino como disacáridos, es decir, sacarosa, maltosa y lactosa; sobre estos sustratos van a actuar la maltasa y alfa- dextrinasa; las disacaridasas como sacarasa y la lactasa que son enzimas intestinales que extienden la sacarosa y la lactosa en monosacáridos absorbibles fácilmente.
Fase II
Cuando los monosacáridos son absorbidos, principalmente la glucosa y la pequeña cantidad de galactosa y fructosa que se convierten en glucosa en el hígado entran a la célula para producir energía, casi la totalidad de los carbohidratos se usan con esta finalidad. En el cuerpo humano, se adquiere la energía en mayor parte de la producción celular-mitocondrial de adenosín trifosfato O ATP de manera abreviada.
Para obtener energía, es importante que la glucosa ingrese a la célula; lo cual realiza por difusión facilitada que se basa en el principio de paso de una sustancia de concentración mayor a concentración menor, aunque se distingue de la difusión simple ya que necesita de una proteína de transmembrana transportadora de glucosa o también denominado GLUT. Así la glucosa ingresa al citoplasma celular por medio del proceso de difusión facilitada.
El carbono 6 de la glucosa (C6H12O6) dentro del citosol se fosforila obteniendo glucosa-6-fostato que es posible por la acción enzimática de la glucocinasa que está en el hígado y de la hexocinasa; la glucosa de este modo no va a ser capaz de escapar de la célula porque donde se une con el radical fosfato es definitivo, con excepción en el hígado, células epiteliales del intestino y epitelio tubular del riñón donde la enzima glucosa-fosfasa logra romper la unión con el radical fosfato y posibilita la salida a través de la célula de la glucosa.
Fases de la producción de ATP
Glucólisis citosólica por el ciclo de Embden Meyerhof
La glucosa (C6H12O6) se va a dividir en dos moléculas de ácido pirúvico (C3H6O3) por medio de la piruvato deshidrogenasa. Este procedimiento no depende directamente del oxígeno (O2) aunque posteriormente las fases mitocondriales si lo van a hacer, por lo tanto, la acumulación de ácido pirúvico en condiciones de anaerobiosis o paso limitante podrían parar la maquinaria energética celular.
En estas condiciones esparce el ácido pirúvico, conocido también como efecto desagüe, donde se transforma en ácido láctico o lactato a través de LDH, es decir, la lactato deshidrogenasa, de esta manera es posible la sobrevivencia de las células en condiciones extremas. Esta reacción va a producir las moléculas de piruvato, dos ATP y cuatro átomos de hidrógeno, que para generar energía se van a oxidar. Quedando así el producto final acetil CoA + 2 CO2 + 4H.
Ciclo de Krebs
El ácido oxalacetato se mezcla con la acetil CoA obteniendo de esta manera ácido cítrico en la membrana externa mitocondrial donde se genera el ciclo y, después una serie de sustancias diferentes que finalizan con la neoformación de oxalacetato y, de esta manera, con el reinicio del ciclo. Lo importante para tener en cuenta de este ciclo es que, a pesar de que se produce poco ATP, específicamente dos moléculas (una por cada piruvato), se generan dieciséis átomos de hidrógeno (16 H) que, al igual que sucede con las reacciones anteriores, luego va a generar ATP 4 CO2 + 2CoA + 2 ATP + 16H.
Fosforilación oxidativa
Los procesos metabólicos anteriores son muy complejos, involucran a un número importante de enzimas y producen vrios compuestos; sin embargo, la producción de energía, teniendo en consideración las cantidades de ATP, es bastante poca, es decir, apenas cuatro moléculas (dos en la glucolisis y dos más en el ciclo de Krebs). Por esto la fosforilación oxidativa a suplir esta carencia usando veinticuatro átomos de hidrógeno que se generaron en las fases anteriores.
En este proceso los átomos de hidrógeno se oxidan a través de enzimas mitocondriales, lo cual llega a producir solo un electrón y un hidrogenión de cada hidrógeno; los electrones se mezclan con O2 para crear el radical oxidrilo que se va a unir al hidrogenión y creará agua o H2O. En este procedimiento, la producción de energía es gigante.
El procedimiento específico que puede lograrlo es llamado mecanismo quimiosmótico, cuya finalidad va a ser fundamentalmente que los protones puedan pasar a través de una gran ATPasa y así la energía brindará la oportunidad que el ADP se transforme en ATP que llega al citosol a través de difusión simple por medio de la membrana mitocondrial externa y difusión facilitada por medio de la membrana mitocondrial interna.
Liberación anaeróbica de energía
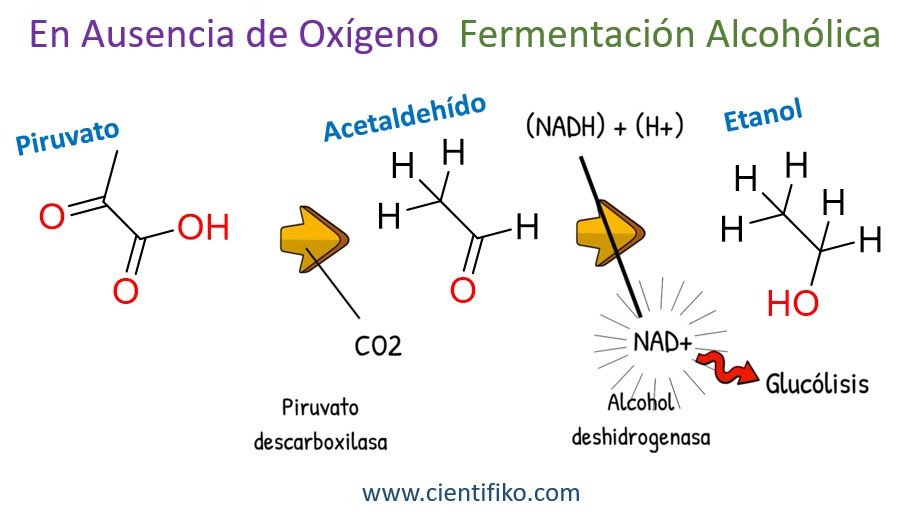
En condiciones anaerobias donde no se dispone de oxígeno solamente se realiza la glucolisis con la formación de piruvato, es decir, no se usan las vías mitocondriales de generación de energía. Debido a que esta reacción no requiere oxígeno, es muy ineficiente ya que usa solamente 24.000 calorías para sintetizar adenosín trifosfato o ATP por cada molécula de glucosa metabolizada, el equivalente 3% de la energía completa que posee una molécula de glucosa; no obstante, este procedimiento hace posible la supervivencia celular por unos minutos cuando no se cuenta con oxígeno.
Si se tiene en cuenta la ley de masas, el resultado de todo el proceso de la glucolisis son específicamente el piruvato producido y los átomos de hidrógeno, el cúmulo de alguno de los sustratos mencionados conduce a que las células se inactiven y, posteriormente a la apoptosis; este es el motivo por el cual el ácido pirúvico obtenido se transforma en ácido láctico, a través de la deshidrogenasa láctica. Así la producción de lactato se vuelve necesaria y permite una expansión celular que impide que se forme la acumulación de piruvato.
Reconversión del ácido láctico en piruvato
El metabolismo anaerobio se detiene luego de que se reestablece el aporte de oxígeno, el ácido láctico se transforma en piruvato y comienza de nuevo la sucesión de reacciones. Es necesario hablar del miocardio que es el órgano que tiene la capacidad de transformar el ácido láctico en pirúvico y, de esta forma, mantiene su eficiencia energética en condiciones de anaerobiosis. Esto ocurre ya que este órgano está habituado a condiciones parecidas como las que se producen al realizar ejercicio de alta intensidad.
Los transportadores de monocarboxilato
Haciendo mención del ejercicio de alto impacto, a partir de tres mecanismos por medio del sarcolema se transporta el lactato. Primero las proteínas monocarboxiladas o MCT dirigen el lactato por medio de un sistema de cotransporte que se une a un hidrogenión positivo, situación que es muy importante en relación con la regulación del equilibrio ácido base. Luego, un intercambiador aniónico va a hacer una transformación del lactato por cloro (Cl) o en bicarbonato (HCO3). Y por último ocurre la difusión de lactato no disociado.
Entonces cuando se realiza actividad física de alta intensidad, la función de los trasportadores es realizar el transporte intracelular sin haberse transformado en piruvato introduciendo el lactato a la mitocondria, con la intención de convertirlo en piruvato por medio de la enzima LDH mitocondrial y poder producir energía ingresando a los ciclos de energía o extrayendo lactato del músculo para trasladarlo al hígado, riñón, entre otros músculos para procesar la glucosa.
Enfoque traslacional
Es importante comentar sobre las disacaridasas, y ocurre que la inhibición de algunas de estas enzimas puede retrasar la hidrólisis de los hidratos de carbono y este hecho se ha transformado en una importante alternativa en el tratamiento de la diabetes mellitus tipo 2, se ha podido comprobar que logra reducir significativamente los valores de hemoglobina glucosilada.
Las proteínas transportadoras transmembrana de glucosa o GLUT, en especial el tipo 4, se encuentran afectadas en la diabetes tipo 2 produciendo lo que se denomina resistencia a la insulina que se ha transformado en un objetivo para la farmacología; un medicamento denominado rosiglitazona que activa los receptores de la proliferación de peroxisomas o PPAR, controla y regula eficientemente la resistencia a la insulina; pero sus secuelas son adversas cardiovasculares lo pueden hacer controversial.
Así que cualquier inhibición enzimática en la glucolisis o en el ciclo de Krebs, permitirán que sin importar la presencia de una cantidad de glucosa y oxígeno adecuada no se termine de obtener una porción conveniente de ATP; lo que va a derivar en un cúmulo de piruvato y producción de lactato en circunstancias donde no hay oxígeno que va a responder a una etiología diferentes como se puede mencionar intoxicación por cianuro de potasio o encefalomiopatía mitocondrial.
El ácido láctico, a pesar de que es una herramienta que evita la parálisis energética celular, cuando se aumenta por un periodo largo de tiempo y no se elimina durante las primeras seis horas a partir de la recuperación de una persona enferma, se transforma en un agente predictor de mortalidad de confianza.

La glucólisis y el cáncer
Varias de las células cancerígenas presentan un incremento en la toma de glucosa y del flujo glucolítico. Los tumores en los pacientes que padecen de cáncer crecen bastante rápido, razón por la cual los vasos sanguíneos se van a encontrar en hipoxia. De esta manera, el suplemento energético que tienen las células va a depender fundamentalmente de la glucólisis anaeróbica.
Por otro lado, es cierto que este fenómeno es posible por la intervención de un factor de transcripción inducible por hipoxia o HIF, que llega a aumentar la expresión de las enzimas glucolíticas y transportadores de glucosa en la membrana por medio de otros mecanismos más complejos. (2)
El origen de la acidez en la glucolisis anaerobia
Se ha demostrado por varios estudios que se produce acidez cuando se cataboliza glucosa de manera anaerobia en el organismo del ser vivo. Un grupo de científicos mantienen la idea de que la hidrólisis del ATP es la causa de los hidrogeniones y otro grupo sigue la teoría de que agua es la que brinda los hidrógenos para mantener de esta manera la electroneutralidad en el proceso al crecer la acumulación de aniones, por ejemplo, cuando se generan grandes cantidades de lactato.
Aunque se tiene suficiente evidencia que contradice de que es a partir de la formación de ácido láctico por la lactato deshidrogenasa lo que termina de justificar la acidificación en los momentos cuando sucede este tipo de glucólisis, se explica continuamente esta teoría sin realizar alguna aclaración al respecto. Hay entonces dos grupos que siguen teorías diferentes que consideran que el fundamento de los hidrogeniones en la glucólisis en ausencia de oxígeno es específicamente la hidrólisis del adenosín trifosfato.
Una corriente apoya la idea de que la formación de los hidrogeniones se encuentra relacionada a la obtención de lactato y por esta razón sostienen que aquello que se produce es ácido láctico porque cuando se crea un lactato se origina al mismo tiempo un protón por la hidrólisis de una molécula de adenosín trifosfato. Por otro lado, la otra corriente piensa que los hidrogeniones se forman independientemente del lactato, es decir, sin que tenga que existir equimolecularidad entre los hidrogeniones y el lactato formados, sosteniendo que entonces lo que se produce no es ácido láctico.
Un tercer grupo de científicos plantean que la cantidad total de cationes actúa a la reparación que ocurre de forma espontánea cuando se crean modificaciones en la proporción de cargas positivas y negativas a partir del principio de la electroneutralidad, como en los momentos en los cuales se produce lactato en exceso. Entonces todos los productores de hidrogeniones, como es el caso de la hidrólisis del adenosín trifosfato, depende de las disoluciones amortiguadoras que se encuentran a disposición para impedir que en las sustancias presentes dentro y fuera de la célula sucedan mutaciones importantes de la acumulación de hidrogeniones.
Desde el punto de vista de esta corriente, no se puede pretender que los hidrogeniones formados por la hidrólisis del ATP ni por otro proceso se detengan de forma integral en el medio celular sin que se cambie su concentración a través de los sistemas amortiguadores.
La acidez relacionada con la anaerobiosis va a ser la consecuencia de la relación de otros sistemas involucrados, como es el caso de los ácidos débiles y sus bases conjugadas, y la disociación del agua, para reponer las diferencias de carga que crea el proceso glucolítico en condiciones anaeróbicas, por las cargas negativas que están presentes al formarse cantidades altas de lactato y de los metabolitos glucolíticos. La glucosa es el sustrato energético importante para el funcionamiento correcto de los organismos de los seres vivos. (3)
Referencias
(1) Silberberg MS (2003). Chemistry, the molecular nature of matter and change, 3rd ed., McGraw-Hill, Boston, Mass., USA p. 777.
(2) Akram, M. (2013). Mini-review on Glycolysis and Cancer. J. Canc. Educ., 28, 454–457.
(3) Liberman M, Ricer R. Bioquímica, Biología Molecular y Genética,6ta. ed. Wolters Kluwer, Barcelona. 2015.














0 comentarios